真固生物结直肠癌伴随诊断产品多中心千人临床试验结果发布
发布时间:2021-04-27 10:39:30 访问次数:
2021年4月23日~24日HIT第三届热点肿瘤分子诊断技术与应用论坛于上海盛大开幕。作为肿瘤伴随诊断创新企业,真固生物携结直肠癌LC103试剂盒产品亮相本次大会。

真固生物研发总监王博-博士围绕”高通量测序IVD在结直肠癌伴随诊断方面的临床研究”专题展示了最新研究成果并进行报告。
真固生物作为美国pillar biosciences—SLIMamp®(Stem-Loop Inhibition Mediated amplification)多重PCR文库制备技术唯一技术授权合作商,其自主研发出结直肠癌伴随诊断的IVD产品——LC103试剂盒,可检测KRAS/NRAS/BRAF/PIK3CA等关键标志基因的突变。据悉,LC103包含22个目标基因,103个扩增子,对FFPE样本中的SNV和INDEL进行检测,最低起始量可低至2.5ng,最低检测下限可达0.6%,兼容Illumina、MGI和Ion Torrent三大测序平台。该IVD产品已在中美两地独立进行性能验证,平行开展多中心临床队列研究,并分别在NMPA和FDA进行注册申报,预计2021年第二季度可以获得FDA的批准,中国NMPA审批预计在2021年年底之前完成。
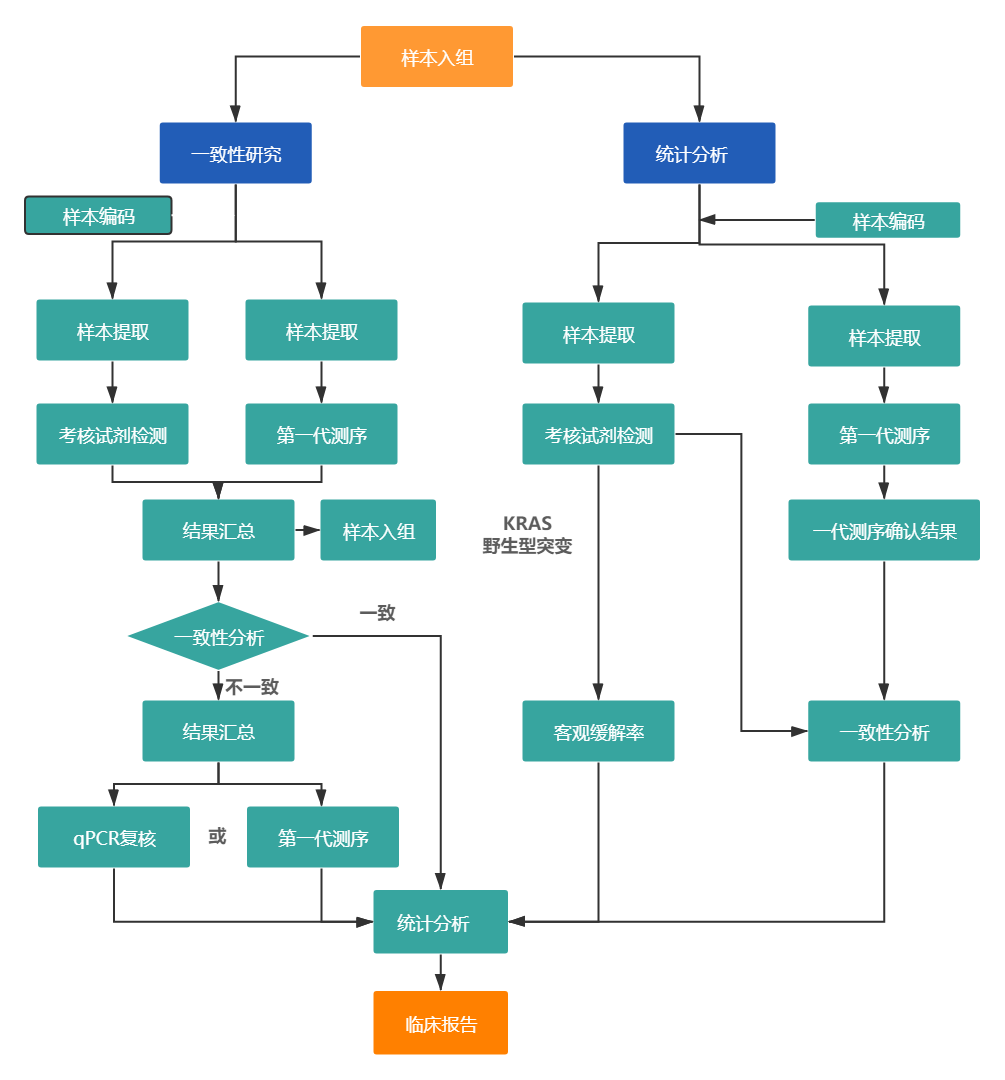
1 性能一致性
在纳入试验的1,106例样本中,共检测出阳性突变样本493例。与金标准检测结果进行比较,各基因的总体符合率均较好,Kappa系数均大于0.9,因此可认为两种方法高度一致,两种方法等效。
2 临床一致性
选取两个中心进行临床一致性研究,考核LC103与已经批准的伴随诊断试剂进行比较。阳性符合率为100.00%,阴性符合率99.36%,总符合率为99.54%。Kappa系数0.9885(> 0.9)说明两种方法检测结果高度一致,两种方法等效。
3 药物关联性评价
选取LC103检测结果为KRAS 野生型突变的样本,按照试验方案考查应受试者“西妥昔单抗”用药的客观缓解率(ORR)。
最终,客观缓解率达到65.38%,说明考核试剂检测结果与伴随药物的关联性较好(可接受范围60%~70%)。
4 基因突变情况
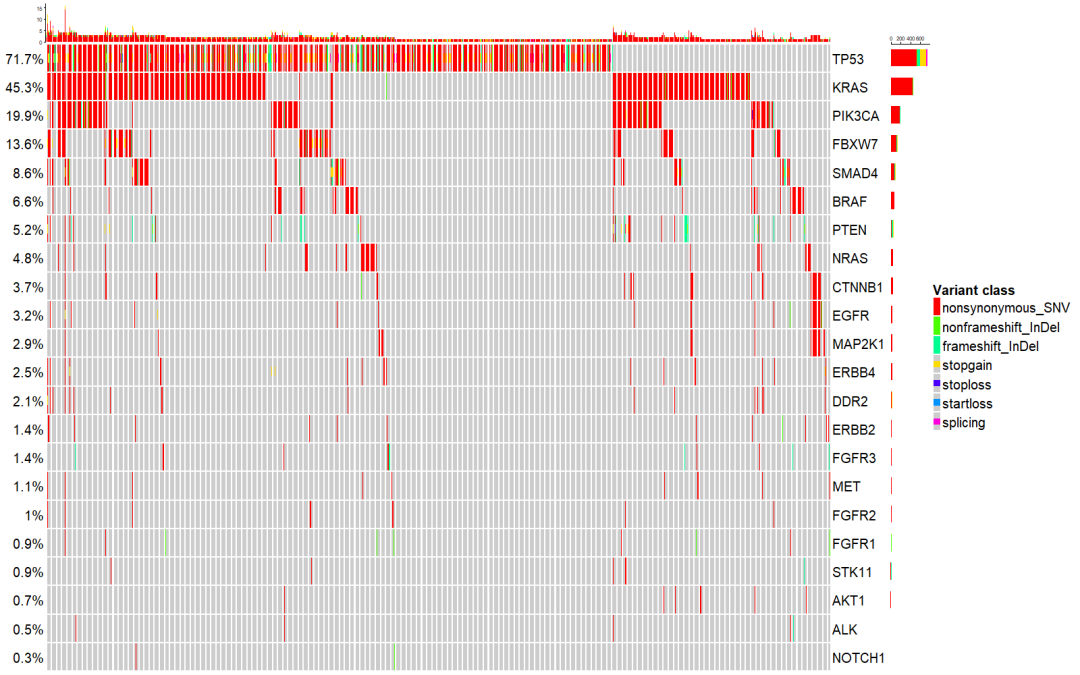
图1.基因突变情况分析
结果显示,在此中国人群结直肠癌队列中,TP53突变占比最高达到71.7%,其次是KRAS为45.3%和PIK3CA为19.9%。另外两个关键标志物NRAS 和 BRAF分别占比为4.8%和6.6%。其中KRAS的变异集中在12和13密码子,BRAF 的变异富集在热点V600E 变异上。考察基因突变之间的关联性发现,KRAS 与BRAF、KRAS 与NRAS 相互排斥,很少同时发生突变(p-value 3.0e-6, 6.1e-5)。
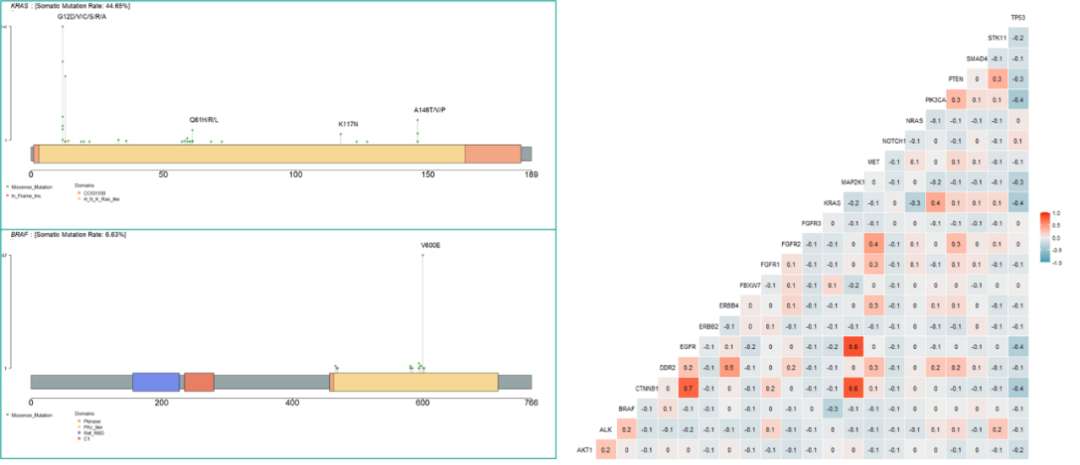
图2.突变基因关联性分析
错配修复通路完整的病例(412)占总病例(596)的68.9%,经计算发现PIK3CA和TP53 的突变在这些病例中富集。结合MMR状态以及PIK3CA等关键标志物的突变信息,可以用于鉴别特定病人亚群,对用药具有指导意义。
利用多中心千人临床研究验证了真固生物LC103试剂盒在一致性与伴随药物的关联性上均满足结直肠癌临床伴随诊断的要求; 结直肠癌主要突变集中在TP53、KRAS 和PIK3CA基因 BRAF、NRAS人群突变频率在中美人群中差异较大 美国人群BRAF 突变频率(~12%)约是中国的2倍 NRAS 整体频率都很低但中国(~5%)约是美国的2倍 KRAS 突变主要集中在12、13密码子,BRAF 的突变主要热点为V600E PIK3CA 基因的突变位点在中美之间差别较大 美国人群中突变频率最高的I391M在中国人群中几乎不发生 中国人群中突变频率最高的是H1047R KRAS 与NRAS、BRAF、PIK3CA的突变互相排斥 BRAF 的突变与肿瘤的分化程度密切相关,PIK3CA 的突变与错配修复通路相关
此外,王博博士表示,真固生物致力于长期持续地建设和完善以多重扩增技术为核心的NGS建库及生信分析技术平台、产品平台以及服务支持平台。在自研多重扩增NGS技术平台的基础上,既持续地推出以注册IVD为核心的NGS系列标准产品及IVD-LDT-RUO多层级定制服务,也为高性价比、高难度价格比要求的细分市场提供临检服务,最终实现为公众提供便捷的、价格可接受的二代测序产品和服务的目标。

 021 - 6089 0178
021 - 6089 0178